上海金畔生物科技有限公司代理New England Biolabs(NEB)酶试剂全线产品,欢迎访问官网了解更多产品信息和订购。
产品信息
PNGase F 是去除糖蛋白中几乎所有 N-连接寡糖的最有效的酶促法。PNGase F 可将天冬酰胺残基脱氨基为天冬氨酸,从而切出完整的寡糖,后者可用于进一步分析。某些植物和昆虫的寡糖中含有一个通过 α(1-3) 键与核心糖链相连的岩藻糖,这种结构可抵抗 PNGase F 的切割活性。
要去除 O-连接糖链,必须通过一系列糖苷外切酶去除单糖,直到附着在丝氨酸或苏氨酸上的核心仅剩 Galβ1-3GalNAc(核心 1)和/或 GlcNAcβ1-3GalNAc(核心 3)为止。NEB O-糖苷酶克隆自粪肠球菌(Enterococcus faecalis),可以去除这些没有修饰的丝氨酸或苏氨酸残基的核心结构。任何对核心结构的修饰,包括唾液酸化,都会阻断 O-糖苷酶的作用。唾液酸残基很容易被 α2-3,6,8,9 神经氨酸苷酶 A 去除。此外,可在去糖基化反应中加入 β(1-4) 半乳糖苷酶 S 和 β-N-乙酰氨基己糖苷酶 f 等糖苷外切酶,以便去除存在于核心结构上的其它复杂修饰。这种酶结合可能无法去除所有 O-连接寡糖,但应能去除许多常见的寡糖结构。
蛋白去糖基化混合液 II 包含去除所有 N-连接、简单 O-连接糖链以及一些复杂 O-连接糖链所需的所有酶、试剂和对照品。该产品中的酶能用于 20 次反应或处理 2 mg 糖蛋白。蛋白去糖基化混合液 II 中包含的所有酶和试剂都与质谱兼容。在去糖基化处理后,样品可直接进行质谱分析。
图 1: 经 O-连接和 N-连接糖基化修饰的糖蛋白。
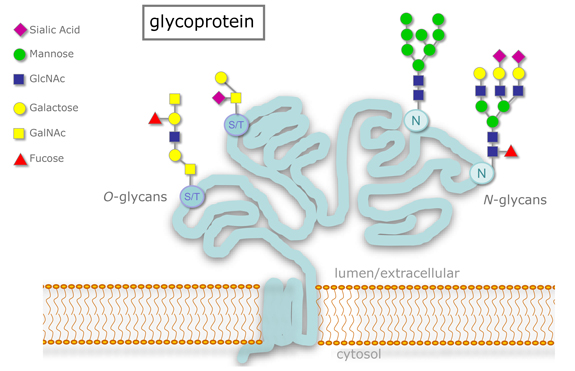
图 2
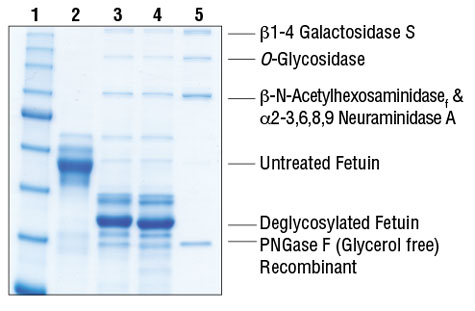
泳道 1:彩色预染蛋白 Standard,宽范围(11-245 kDa)(NEB #P7712)
泳道 2:20 μg 未处理的胎球蛋白对照
泳道 3:20 µg 胎球蛋白使用去糖基化混合缓冲液 1 在非变性条件下去糖基化
泳道 4:20 µg 胎球蛋白使用去糖基化混合缓冲液 2 在变性条件下去糖基化
泳道 5:5 µl 蛋白去糖基化混合液 II
蛋白去糖基化混合液 II:
PNGase F(无甘油),重组酶:
10,000 unit/管
O-糖苷酶:
80,000 unit/管
α2-3,6,8,9 神经氨酸苷酶 A:
400 unit/管
β1-4 半乳糖苷酶 S:
960 unit/管
β-N-乙酰氨基己糖苷酶f:
300 unit/管
底物对照:
胎球蛋白,0.5 mg(含有唾液酸化的 N-连接和 O-连接糖链)
蛋白去糖基化混合液 II 中包含以下酶
O-糖苷酶(NEB #P0733)又称 α-N-乙酰氨基半乳糖苷内切酶,是克隆自粪肠球菌(Enterococcus faecalis)的重组酶(1)。该酶可以从糖蛋白中切除核心 1 和核心 3 型 O-连接二糖。分子量约 147 kDa。
PNGase F(无甘油),重组酶(NEB #P0709),也称为肽:N-糖苷酶 F,克隆自米尔伊丽莎白菌(Elizabethkingia miricola,旧称 Flavobacterium meningosepticum),在 E. coli 中表达(2)。PNGase F(无甘油),重组酶是一种酰胺酶,可以在无 α(1-3) 岩藻糖基化的 N-连接糖蛋白的高甘露糖型、杂合型和复合型寡糖最内侧 GlcNAc 和天冬酰胺残基之间进行切割。分子量约 36 kDa。
α2-3,6,8,9 神经氨酸苷酶 A(NEB #P0722)又称唾液酸酶 A,是一种克隆自产脲节杆菌(Arthrobacter ureafaciens)的重组酶,在 E. coli 中表达(3)。该酶可催化水解糖蛋白和寡糖中 α2,3、α2,6、α2,8 和 α2,9 连接的 N-乙酰神经氨酸残基。分子量约 100 kDa。
β1-4 半乳糖苷酶 S(NEB #P0745)是一种克隆自肺炎链球菌(Streptococcus pneumoniae)的重组酶,在 E. coli 中表达(4)。该酶是一种具有高度特异性的糖苷外切酶,催化水解寡糖上 β1-4 连接的半乳糖残基。分子量约 231 kDa。
β-N-乙酰氨基己糖苷酶 f(NEB# P0721)是一种克隆自褶皱链霉菌(Streptomyces plicatus)(5)的重组酶,在 E. coli 中过表达(6)。该酶可催化水解寡糖末端 β-N-乙酰氨基半乳糖和氨基葡糖残基。分子量约 100 kDa。
- 产品类别:
- Exoglycosidases Products,
- Endoglycosidases Products,
- Proteome Analysis Products
- 应用:
- Expression Systems,
- Glycan Sequencing,
- Protein Digestion,
- Recombinant Glycoprotein Expression,
Glycoprotein Analysis
-
产品组分信息
本产品提供以下试剂或组分:
NEB # 名称 组分货号 储存温度 数量 浓度 -
P6044S -20 Protein Deglycosylation Mix II P6044SVIAL -20 1 x 0.1 ml 20 reactions Deglycosylation Mix Buffer 1 B6044SVIAL -20 1 x 1 ml 10 X Deglycosylation Mix Buffer 2 B6045SVIAL -20 1 x 1 ml 10 X Fetuin P6042SVIAL -20 1 x 0.05 ml 10 mg/ml
-
-
特性和用法
贮存溶液
50 mM NaCl
20 mM Tris-HCl
2.6 mM EDTA
pH 7.5 @ 25°C热失活
65°C for 20 minutes
-
优势和特性
应用特性
蛋白去糖基化混合液 II 包含去除所有 N-连接、简单 O-连接糖链以及一些复杂 O-连接糖链所需的所有酶、试剂和对照品。该产品中的酶能用于 20 次反应或处理 2 mg 糖蛋白。蛋白去糖基化混合液 II 中包含的所有酶和试剂都与质谱兼容。
-
相关产品
相关产品
- p0709-pngase-f-glycerol-free-recombinant
- p0733-o-glycosidase
- α2-3,6,8,9 神经氨酸苷酶 A
- β1-4 半乳糖苷酶 S
- β-N–乙酰氨基己糖苷酶 f
- α1-2 岩藻糖苷酶
- α1-3,4 岩藻糖苷酶
- β1-3 半乳糖苷酶
- α-N-乙酰半乳糖胺酶
-
注意事项
- 蛋白去糖基化混合液 II 提供两种不同的反应缓冲液。请参考“操作说明、说明书 & 用法”菜单,了解与各个缓冲液系统相关的操作说明。当需要使用非变性条件时,请使用 10X 去糖基化混合缓冲液 1(NEB #B6044)。10X 去糖基化混合缓冲液 2(NEB #B6045)虽会还原糖蛋白,但能实现最高效且最完整的去糖基化水平。如果无需非变性条件,则推荐使用 10X 去糖基化混合缓冲液 2。
- 不建议将蛋白去糖基化混合液 II 用于粘蛋白样底物。
-
参考文献
- Koutsioulis, D. Landry, D. and Guthrie, E.P. (2008). Glycobiology. 18, 799-805.
- Plummer, T.H. Jr. and Tarentino, A.L. (1991). Glycobiology. 1, 257-263.
- McLeod, E. New England Biolabs, Inc. Unpublished observation
- Chen, M. New England Biolabs, Inc. Unpublished observation
- Robbins, P. et al. (1992). Gene. 111, 69-76.
- Guan, C. and Wong, S. New England Biolabs, Inc. Unpublished observation
操作说明、说明书 & 用法
-
操作说明
- Reaction Protocols for Protein Deglycosylation Mix II (P6044)
-
应用实例
- Analysis of a Fusion Protein using the Protein Deglycosylation Mix II and Mass Spectrometry
工具 & 资源
-
选择指南
- Endoglycosidase Selection Chart
FAQs & 问题解决指南
-
FAQs
- What is the difference between the discontinued Protein Deglycosylation Mix (NEB# P6039) and the new Protein Deglycosylation Mix II (NEB# P6044)?
- Two different reaction buffers (10X Deglycosylation Mix Buffer 1 and 2) are supplied with the Protein Deglycosylation Mix II. How do I know which buffer to use?
- Are downstream analysis such as HPLC and Mass Spectrometry compatible with the Protein Deglycosylation Mix II?
- I tried the Protein Deglycosylation Mix II on my glycoprotein and didn’t see removal of the carbohydrate. What could be the problem?
- How much Protein Deglycosylation Mix II should I use to remove the carbohydrates under native (non-denaturing) conditions?
- What is a good control substrate for the Protein Deglycosylation Mix II?
- Are Protease Inhibitors acceptable for use with the Protein Deglycosylation Mix II reaction?
